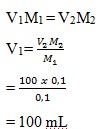Latihan 8. Buatlah 4 soal pilihan ganda dari tugas kelompok anda.
a. 2 – log 4
b. 2 + log 4
c. 2 + log 2
d. 12 + log 4
e. 12
Pembahasan:
H2SO4 merupakan asam kuat, bervalensi 2
[H+] = Ma x Val
= 0,02 x 2 = 4 x 10-2
pH = -log 4 X 10-2
= 2-log 4
Jawaban: A
2.Berapakah konsentrasi ion [OH–] dalam larutan jika konsentrasi H+ = 2 X 10-4 M (Diketahui Kw = 10-14)…….
a. 5 X 10-10
b. 5 X 10-18
c. 0,2 X 10-10
d. 0,2 X 10-8
e. 2 X 10-10
Pembahasan:
Dalam larutan dengan pelarut air, berlaku :
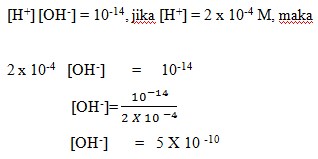
jawaban a
3. Perhatikan data pengujian pH beberapa sampel air limbah berikut!
| Jenis air limbah | P | Q | R | S | T |
| pH | 8 | 5,5 | 7,6 | 9,4 | 4,7 |
Air limbah yang tercemar asam adalah . . . .
a. P dan Q
b. Q dan T
c. R dan S
d. S dan T
e. T dan R
Pembahasan:
Nilai pH untuk asam <7 sehingga berdasarkan data diatas dapat diketahui air limbah yang tercemar asam adalah Q dan T
Jawaban: B
4.Untuk menetralkan 100 mL larutan KOH 0,1 M diperlukan larutan H2SO4 0,1 M sebenyak…..
a. 10 mL
b. 50 mL
c. 100 mL
d. 150 mL
e. 200 mL
Pembahasan :